其實後面牽涉了一個名為「共晶反應」的基礎原理,我會說共晶是發生原料融化原因,而共熔是釉藥因此而產生的表現。
共晶反應(Eutectic reaction)是一種在冷卻凝固過程中發生的熱力學現象,當多成分液體降溫時,會在特定溫度下同時生成兩種(二元系統)或三種(三元系統)固相。
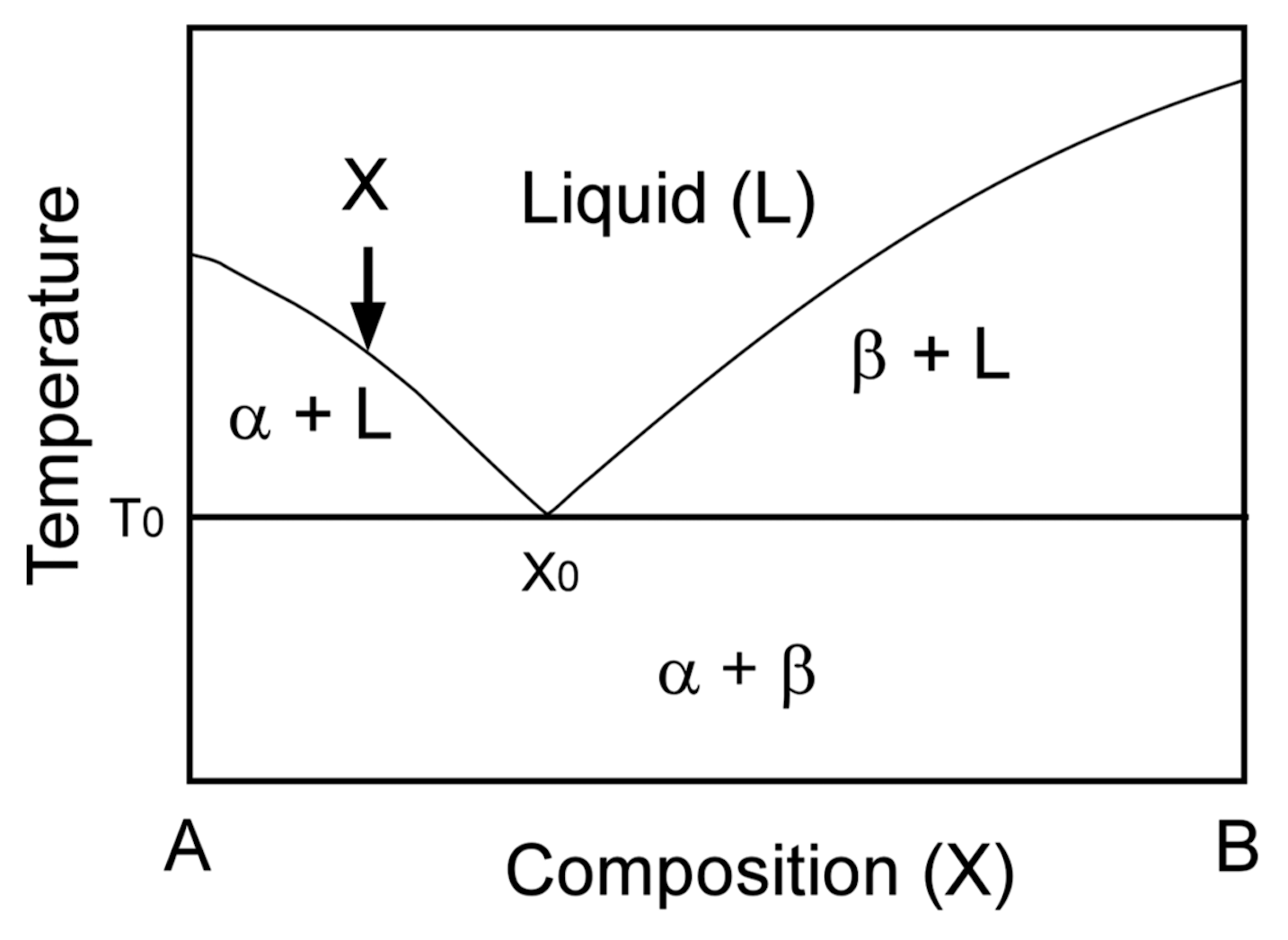
在二元共晶系統中(如圖一[1]),由兩種成分 A 與 B 所構成。當 A 中加入 B 時,A 的熔點會下降;反之亦然,因此在某一特定組成下會出現整個系統的最低熔融溫度,稱為共晶溫度(eutectic temperature)。當液體冷卻時:若成分偏向 A(亞共晶,hypoeutectic),會先析出 α 初晶相;隨著溫度降低,剩餘液體逐漸富含 B;到達共晶溫度時,剩餘液體同時形成 α 與 β 兩種固相完成凝固。
若成分正好位於共晶組成,則 α 與 β 會同時由液體中析出,形成細密且均勻的共晶組織。
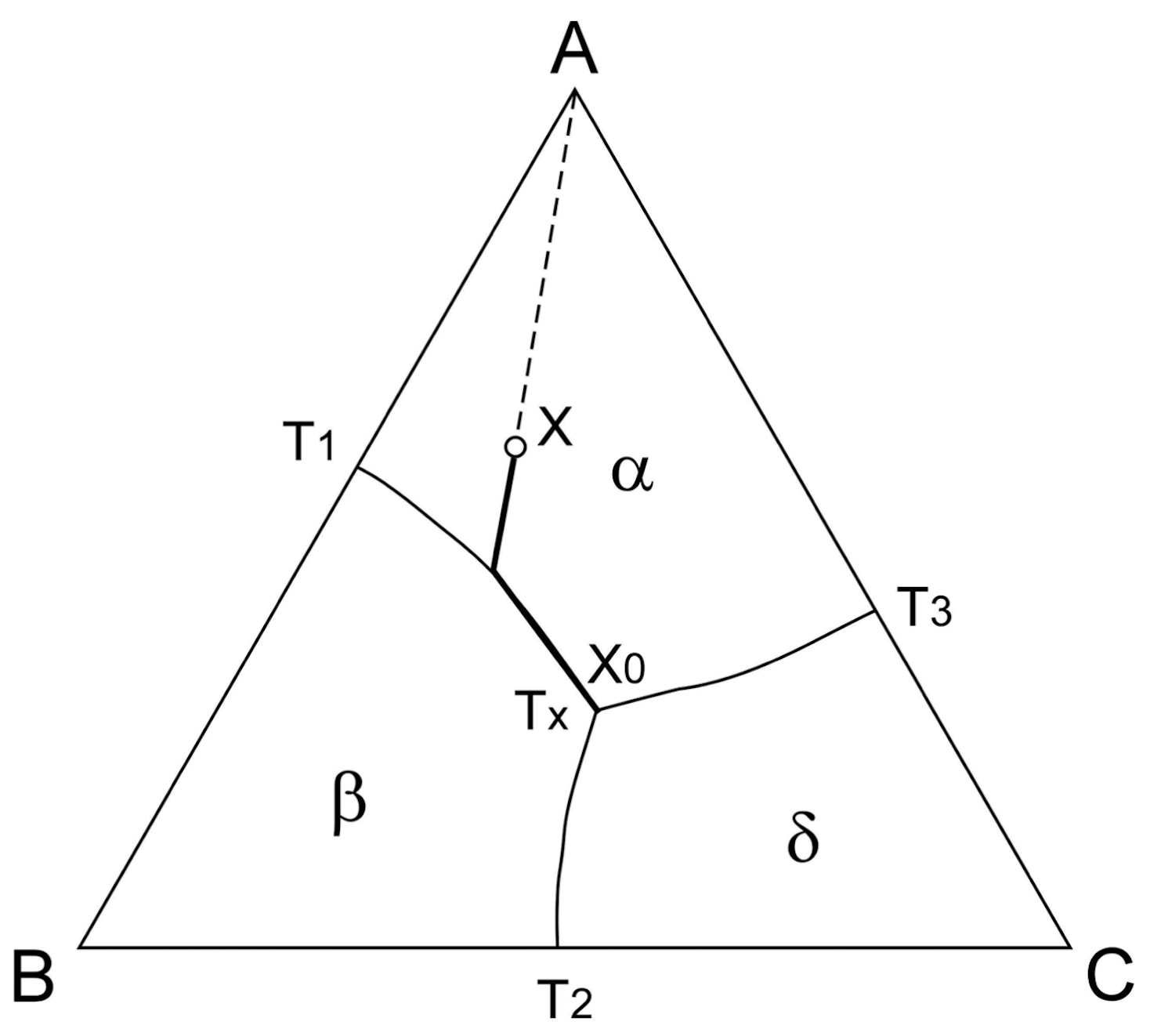
在三元共晶系統中(如圖二[1]),液體包含 A、B、C 三種成分。不同成分區域會先析出不同的初晶相(α、β 或 δ)。隨著冷卻:首先生成某一主要初晶相;
液體組成沿著二元共晶線改變;最後在三元共晶溫度下,同時形成三種固相的三元共晶組織。
透過改變組成比例,可以得到:
粗大的初晶相分散於共晶基質中,或由多種細緻共晶結構混合而成的複合材料。
而這個現象跟陶瓷的關聯在於:釉藥的熔融行為本質上就是多元共晶系統,只是陶藝上通常不直接用「共晶」這個材料科學的名詞來描述。
降低熔融溫度
釉藥中常見:
SiO₂(玻璃質)
Al₂O₃(穩定劑)
助熔劑(Na₂O、K₂O、CaO、B₂O₃ 等)
不同氧化物混合後會形成低於任何單一原料熔點的共晶點
例如:
純 SiO₂ 熔點約 1710 °C
但加入 Na₂O 或 B₂O₃ 後,可在 1000–1200 °C 熔融這正是二元或三元共晶降低熔點的結果。釉藥能在窯燒溫度熔融,事實上就是利用共晶反應。
而共晶的比例會決定了:
- 熔融開始溫度
- 黏度下降速度
- 燒成的溫域
- 熔融程度加快
- 流動性大幅提升
- 容易過熔導致流釉或是起泡
偏離共晶點時:
熔融溫域變寬(意思就是熔點又升高了)釉較穩定,這也是為什麼有些釉在某些原料只差1–2% 的情況下就就流釉或變成無光。
而現代釉藥幾乎都是三元共晶或是多元共晶:
例如最常見的:
- KNaO–CaO–SiO₂
- CaO–MgO–Al₂O₃–SiO₂
所以看完這篇的你就知道以後在調釉以及燒成時就知道會因此融化就是因為我們調的原料比例接近共晶組成,所以形成更低的熔點,而出現共熔現象啦!
【1】 Goto, T., & Tu, R. (2019). Eutectic ceramic composites by melt-solidification. Journal of the Korean Ceramic Society, 56(4), 331-339.
【2】 Callister Jr, W. D., & Rethwisch, D. G. (2020). Materials science and engineering: an introduction. John wiley & sons.
以上文章經過資料考究並結合自身經驗而撰,若有遺漏疏失或錯誤歡迎各位先進到聯絡我們指教,謝謝!

